Hogyan számoljuk ki a tömegszázalék
Mass százalékos meghatározza a százalékos elemek egy kémiai vegyület. [1] Annak megállapításához, a tömegszázalék szükséges tudni, hogy a molekulatömeg (g mólonként) tartalmazza a csatlakozó elemek számát vagy gramm minden egyes komponens megszerzéséhez szükséges egy adott oldatban. [2] Az tömegszázalék számított igen egyszerű: elegendő, hogy osztja a tömeg elem (vagy komponens) az összesített tömege a vegyület (vagy oldat).
lépések szerkesztése
1. módszer a 2:
A tömegszázalékos értékek meghatározása Egy adott tömeg szerkesztése


- Elején a probléma megoldásának, rögzíti a egyenlőség tömegszázaléka = (komponens tömegének / teljes tömegének vegyület) x 100.
- A tömeg összetevője érdeklik kell a problémát. Ha a tömeg nem adott, menj a következő fejezetet, amelyben arról beszélt, hogyan határozza meg a tömeg- az ismeretlen tömeget.
- A teljes tömege a kémiai vegyületet kapunk hozzáadásával a tömegek minden elemét (komponensek), amelyek részei ennek a vegyületnek (vagy oldat).
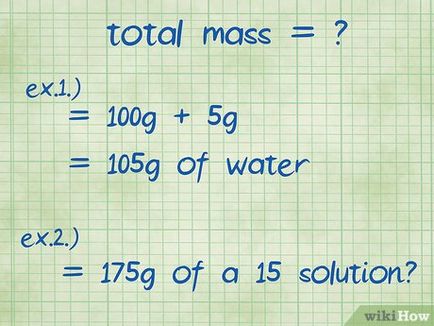
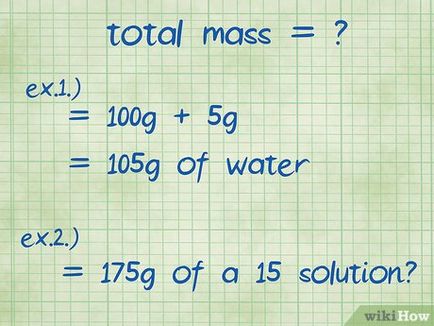
- 1. példa: Mi tömegszázalékának 5 g nátrium-hidroxidot feloldunk 100 g vízben?
- A teljes tömege az oldat az összege mennyiségű nátrium-hidroxid és a víz: 100 g + 5 g így 105 g
- 2. példa: Hogyan sok nátrium-klorid és víz előállításához szükséges 175 g 15 százalékos oldat?
- Ebben a példában, mivel a teljes tömeg és a szükséges százalékos, és szeretné megtalálni a hatóanyagok számával kell az oldathoz. A teljes súlya 175 g.


- 1. példa: Az előre meghatározott tömegű komponenseket - nátrium-hidroxid - 5 gramm.
- 2. példa: Ebben a példában egy adott súlya a komponens ismeretlen, és meg kell találni.
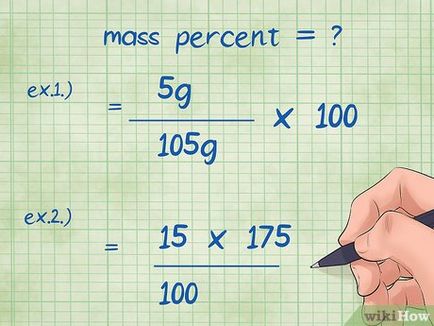
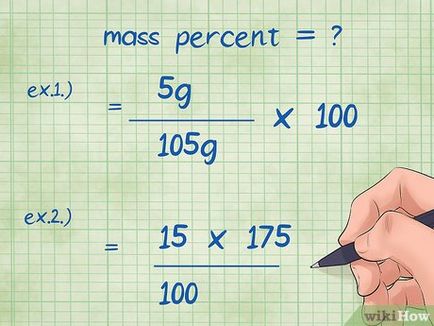
- 1. példa: tömegszázalék = (ü komponens / teljes tömege a vegyület) x 100 = (5 g / 105 g) x 100.
- 2. példa át kell alakítani egy általános képletű tömegszázalék úgy, hogy képes legyen megtalálni az ismeretlen tömege kémiai komponens: komponens = tömeg (tömeg százalékában teljes tömege a vegyület *) / 100 = (15 * 175) / 100.
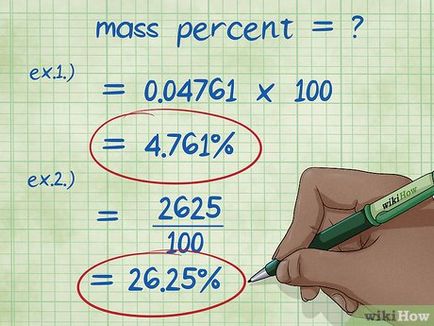
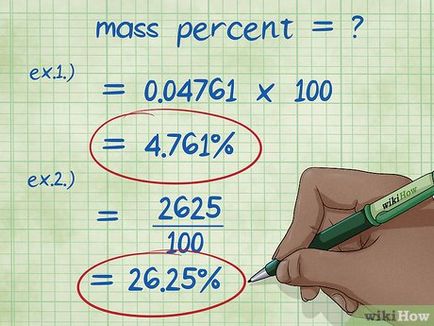
- 1. példa: (5/105) x 100 = 0,04761 x 100 = 4,761%. Így, a tömegszázalékos 5 g nátrium-hidroxidot feloldunk 100 g víz 4,761%.
- 2. példa: expressziója átírni tömegszázalékának komponens (tömegszázalék a teljes anyag tömege *) / 100, ahol találunk: (15 * 175) / 100 = (2625) / 100 = 26,25 g nátrium-kloriddal.
- Szükséges mennyiségű vizet kivonásával kapott komponens tömegének a teljes tömegére az oldat: 175-26,25 = 148,75 g vizet.
2. módszer 2:
Meghatározása tömegszázaléka, amikor a tömegek nincsenek beállítva szerkesztése


- Elején a probléma megoldásának, rögzíti a egyenlőség tömegszázaléka = (moláris tömege az elem / teljes molekulatömege vegyület) x 100.
- Mindkét érték mérése g mólonként (g / mol).
- Ha nem kapnak nehezék százaléka egy komponens egy adott helyzetre megtalálható a moláris tömeget.
- 1. példa: Find tömegszázalékának hidrogénnek a víz-molekula.
- 2. példa: mekkora tömegű szén aránya a glükóz molekula.


- 1. példa: rekord kémiai képlet vízzel, H2 O.
- 2. példa: Glükóz írási kémiai képlet, C6 H12 O6.


- 1. példa: Find az oxigén moláris tömegét (15,9994) és hidrogén (1,0079). [9]
- 2. példa: Find moláris szén tömege (12,0107), az oxigén (15,9994) és hidrogén (1,0079).
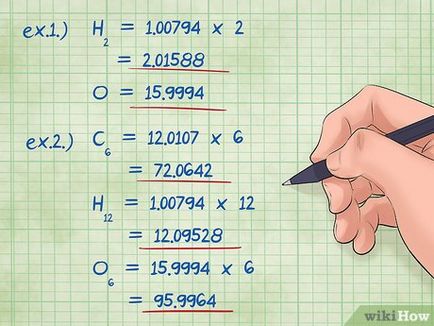
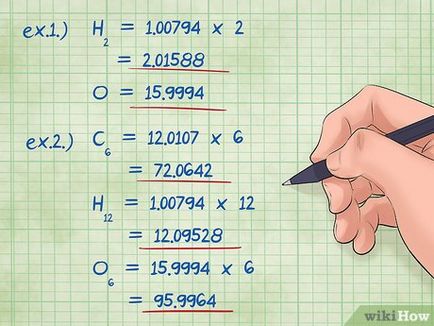
- 1. példa: a hidrogén-szimbólum 2, és oxigénmentes szimbólum 1 (ekvivalens a hiánya). Így a moláris tömege hidrogén meg kell szorozni 2: 1,00794 x 2 = 2,01588; moláris tömege oxigén ugyanaz marad, 15,9994 (azaz, szorozva 1).
- 2. példa: Egy szimbólum áll 6 szénatomos hidrogén alatt 12 és oxigén mellett 6. szorzása moláris tömege elemek ezek a számok, azt találjuk:
- szén: (12,0107 * 6) = 72,0642
- hidrogén: (1,00794 * 12) = 12,09528
- oxigén: (15,9994 * 6) = 95,9964
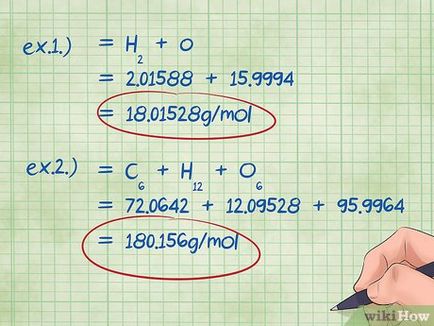
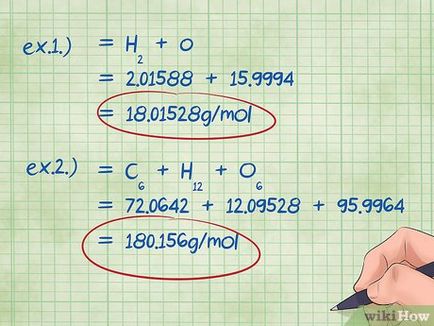
- 1. példa: adjunk hozzá, hogy 2,01588 g / mol (tömege két mol hidrogén atomok) 15,9994 g / mol (súlya egy mól oxigén atomok), ennek eredményeként, akkor 18,01528 g / mol.
- Példa 2-szeres moláris tömegeket eredmények: szén + hidrogén + oxigén = 72,0642 + 12,09528 + 95,9964 = 180,156 g / mol.
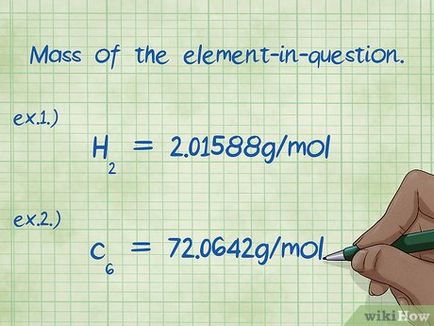
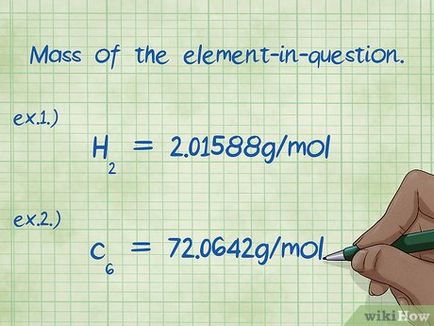
- 1. példa: A tömegét hidrogén a vegyület 2,01588 g / mol (tömege két mól hidrogénatom).
- 2. példa: A szén-ben a vegyület 72,0642 g / mol (mól tömege hat szénatomos).


- 1. példa: tömegszázalék = (moláris tömege elem / teljes molekulatömegű vegyület) x 100 = (2,01588 / 18,01528) x 100.
- 2. példa: tömegszázalék = (moláris tömege elem / teljes molekulatömegű vegyület) x 100 = (72,0642 / 180.156) x 100.
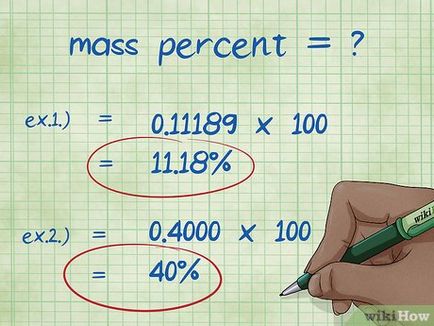
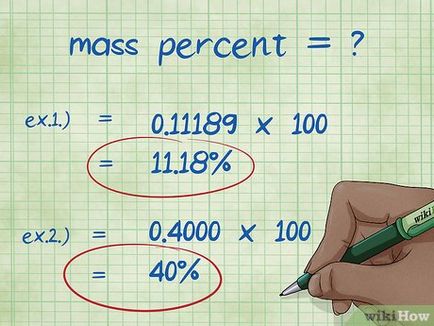
- 1. példa: tömegszázalék = (moláris tömege elem / teljes molekulatömege vegyület) x 100 = (2,01588 / 18,01528) x 100 = 0,11189 x 100 = 11,18%. Így a tömegszázaléka a hidrogénatomokat egy molekula víz egyenlő 11,18%.
- 2. példa: tömegszázalék = (moláris tömege elem / teljes molekulatömege vegyület) x 100 = (72,0642 / 180.156) x 100 = 0,4000 x 100 = 40.00%. Így a tömeg százalékos szénatomot tartalmaznak a glükóz molekula 40,00%.