Kémiai tulajdonságait karbonsavak és előállítására szolgáló eljárások
Monobázisos karbonsavakkal álló szénváz és csak egy karboxil funkciós csoportot. Minden diák tudja, kémiai tulajdonságai karbonsavak. 10 képzési osztály kémia program tartalmazza közvetlenül tulajdonságainak tanulmányozására egybázisú savak. Kétbázisos és több-bázisú savak a szerkezetükben két vagy több karboxilcsoportot, ill.
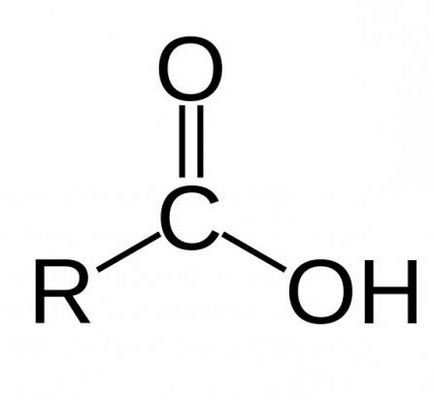
Továbbá, a jelenléte vagy hiánya a kettős és hármas kötések a molekulában lévő telített és telítetlen karbonsavak. Kémiai tulajdonságokat és a különbségeket az alábbiakban tárgyaljuk.
Ha a szerves sav az összetétele csoport szubsztituált atomot, a nevét tartalmazza szubsztituens csoport neve. Így, ha a hidrogénatom helyén halogénatom, a sav is jelen lesz cím nevét halogénatom. Hasonló változások mennek keresztül neve, ha van helyettesítés a kiindulási aldehid, hidroxil- vagy amino-csoportokat.
Izoméria szerves karbonsavak
Gyakorlatilag minden szerves anyag van a képessége, hogy az izomerizációt. A karbonsav sem kivétel. A következő típusú izoméria:
- A szénváz.
- Interclass izomerek.
- régióizomereket;
Izomerizirovatsya lehetőséget, hogy közvetlenül befolyásolják a kémiai tulajdonságait karbonsavak.
Izoméria csontváz lehetséges savak, amelyeknek szénhidrogéncsoport tartalmaz legalább négy szénatomot tartalmaz. Interclass, viszont lehetővé savak két szénatommal az radikális. Egy térbeli képes karbonsavak és csak egyszeres kötések a csontváz.
Számlálás és kritikus karbonsav
A karbonsav: kémiai összetétel
A részletesebb megértéséhez a karbonsavak nézd meg a tulajdonságait. Az iskolai program egy nagy mennyiségű tekinthető egybázisú karbonsavak, kémiai tulajdonságokkal rendelkezik, amelyek megmutatkoznak a reakciókban a hidrogén-halogenid, víz és egyéb anyagok. Az összes ilyen savval:
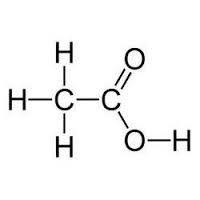
- Disszociálnak oldatban hidrogén-ionokat és egy karboxil-csoport. Ebben az esetben arra utal, hogy egy hangyasav elektrolitok közepes erősségű és gyenge ecetsav, azaz a disszociációs erő csökken le a homológ sor.
- Festettük lakmuszpapír piros.
- Elektromos áram vezetésére áram.
- React halogénekkel: 2RCOOH + Cl2 = 2RCOOCl + 2 HCI.
- Írja be az észterezési reakció egy alkohollal: R-COOH + R'OH = RCOOR „+ H2O.
- Kölcsönhatásba léphet bizonyos fémek: RCOOH + Mg = RCOOMg + H2.
- Reagálhat bázisos oxidok és hidroxidok típusú sóképzésre: RCOOH + NaOH = RCOONa + H2O.
- Reagál sók: RCOOH + Na2CO3 = RCOONa + H2O + CO2.
Ezek a tulajdonságok változásával magyarázható az egybázisú savak karboxilcsoportjának hidroxil, amely az elektronok elmozdulás a legközelebbi szénatom, részlegesen kioltás a pozitív töltés. Ezen túlmenően, a karbonsav, a kémiai tulajdonságait, amelyek a fent leírt, egy kétirányú interakció atomok között.
Kémiai tulajdonságait egyéb monokarbonsavak
A besorolás ismert, hogy van egybázisú telítetlen karbonsav, a kémiai tulajdonságok, amelyek eltérnek a határértéket.
Így a savat egy kettős kötés a szénhidrogéncsoport - egybázisú telítetlen karbonsavak. A kémiai tulajdonságok ilyen savak vannak kifejezve reakciók:
- Mivel a hidrogén-halogenid, de sokkal lassabb korlátok és ellentétes Markovnyikov szabály, mint a karboxilcsoport csökkenti az elektron sűrűsége kettős kötés: R = CH-COOH + HCI = RCL-CH2-COOH.
- Halogénekkel: Br2 + R = -CH-COOH = R-Br-CHBr-COOH.
- Mivel a hidrogén, így szünetek a kettős kötés: H2 + R = CH-COOH = COOH-R-CH.
- Óvatos oxidációnak, így a formáció oxisavakkal: R = CH-COOH + H2O [O] R (OH) -CH (OH) COOH.
- Radical fellépő oxidáció a szakított-molekulák (például propénsav): CH3-CH = C-COOH + H2O [O] CH3COOH + HOOC-COOH.
- Polimerizáció: n COOH- (CH = CH) -R = n (-COOH-CH-CH-R-)
Kémiai tulajdonságok dvukarbonovyh savak
Dikarbonsav szerves savak - egy dikarbonsav. A kémiai tulajdonságok ilyen monokarbonsavak különböznek tulajdonságait. Ez annak a ténynek köszönhető, hogy az erejét a kétbázisú savak egybázisú nagyobb teljesítmény miatt hatására a második, a karboxilcsoport és a hidroxilcsoport. Bár ez a hatás csökken a távolság a szénláncban.
Kétbázisú savak, a következő tulajdonságokkal:
- Dekarboxilezzük savak (például etandinovoy): HOOC-COOH (t) = HOOC + CO2. Fontos tudni, hogy az oxálsav és a maionsav dekarboxileződik sokkal könnyebb, mint mások.
- A formáció a savas sók és a másodlagos: HOOC-R-R-COOK vagy HOOK-R-R-COOK.
- A formáció a teljes és a részleges észterek.
- Malonsav amely hajlamos egy szubsztitúciós reakciót a hidrogén a következő csoportból CH2-szénhidrogéncsoport könnyen helyettesíthető fématomok.
Sók karbonsavak
Sók - olyan szerves vegyületek, melyekben az esetben kiindulási hidrogénatom a hidroxil- és karboxil-csoportok a karbonsav, hogy a fém. Azaz, a szerves savak reakciókhoz a szervetlen bázisokkal vagy sóik képezni képesek karbonsavak sói. Kémiai tulajdonságok, amelyek elő olyan szerves vegyületek sók, használnak az iparban a termelés a háztartási szappan.
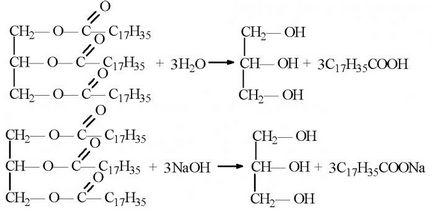
Különösen alkalmas szintézisére a szilárd és folyékony szappanok sztearinsav (oktadekánsav), és a palmitinsav (hexadekánsav). Szintén gyakran használják olajsav (cisz-9-oktadecénsav), és a mirisztinsav (tetradekánsav) savat.
Az alapja reakciót termelő szappanok fölött fekszik észterek szintézisére savak kálium- vagy nátriumsó.
Előállítási módszerei karbonsavak
Módokat és módszereket termelő savak COOH csoport, sok, de a leggyakrabban használt:
- Izolálása a természetes anyagok (zsírok, stb).
- Oxidálva monoalkoholok vagy COH-vegyületek csoportja (aldehidek): ROH (RCOH) [O] R-COOH.
- Hidrolízis lúggal trigalogenalkanov így közbenső monoalkohol: RCl3 + NaOH = (ROH + 3NaCl) = RCOOH + H2O.
- Az elszappanosítási vagy hidrolízisével észter- és alkohol-(észterek): R-COOR „+ NaOH = (R-COONa + R'OH) = r-COOH + NaCl.
- Permanganátos oxidációra alkánok (merev oxidáció): R = CH 2 [O], (KMnO4) RCOOH.
Jelentése karbonsavak az ember és Ipari

Kémiai tulajdonságait karbonsavak nélkülözhetetlen az emberi életet. Ezek nagyon fontos a szervezet számára, mint a nagy mennyiségben minden egyes sejtjében. A zsírok, fehérjék és szénhidrátok mindig áthalad a stádium, amelyben az egyik vagy a másik kapott karbonsavat.
Ezen túlmenően, használt karbonsav létrehozása gyógyszerek. Egyik a gyógyszeripar nem létezhet anélkül, hogy ténylegesen tulajdonságait szerves savak.

A fontos szerepet a vegyület egy karboxil-csoportot, és a játék a kozmetikai iparban. Szintézise zsír az ezt követő előállítását szappanok, mosószerek, háztartási vegyszereket alapján az észterezési reakció karbonsavval.
Kémiai tulajdonságait karbonsavak tükrözi egy ember életében. Ezek, mint a nagy mennyiségben tartalmaz minden cellájában nagy jelentőséget az emberi szervezetben. A zsírok, fehérjék és szénhidrátok mindig áthalad a stádium, amelyben az egyik vagy a másik kapott karbonsavat.