Formula karbonsav Chemistry
A karbonsav - szerves vegyületek, amely molekulák tartalmazhatnak egy vagy több funkciós karboxilcsoportokat-COOH kapcsolódik egy szénhidrogéncsoport.
A karboxil-csoport magában foglalja a karbonil-csoportok> C = O és a kapcsolódó hidroxilcsoport -OH.
Az általános képlet a karbonsav
Az általános képlet a karbonsavak: R-COOH.
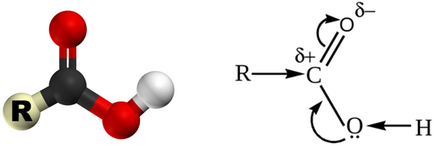
A savas tulajdonságok miatt az elmozdulás a karbonsavak elektronsűrűség, hogy a karbonil-oxigénnel, amely ad okot, hogy a részleges pozitív töltést a hidrogénatom.
Ennek eredményeként, a polaritás a O-H növekszik, és lehetségessé válik a disszociációs folyamat:
A kapott aniont stabilizáljuk töltés delokalizációja:
Alsó karbonsavak, legfeljebb 3 szénatomos alkilcsoport - színtelen folyadék, jellegzetes, átható szag, összekeverjük vízzel bármilyen arányban. A legtöbb tartalmazó savak 4-9 szénatomos - egy olajos folyadék, amelynek kellemetlen szag. Acid, amelyek több mint 10 hidrogénatom - a szilárd anyagok, amelyek vízben oldhatatlan.
A oldhatósága karbonsav ecetsav vízben, és a magas forráspontú társított az intermolekuláris hidrogénkötések. A szilárd állapot karbonsavat létezik többnyire formájában gyűrűs dimerek, mint ahogyan a folyadék és a lineáris kapcsolatot:
Típusai karbonsavak
Attól függően, hogy a szerkezet egy szénhidrogéncsoport, karbonsavak vannak osztva:
- aromás (benzoesav)
- alifás (limit (kapronsav) és telítetlen (akrilsav))
- aliciklusos (kinasav)
- heterociklusos (nikotinsav).
Szerint a karboxilcsoportok száma a karbonsav van osztva:
- egybázisú (ecetsav)
- disav (oxálsav)
- több-bázisú (citromsav).
Amikor be a molekulába más savas funkciós csoportok (. OH, = CO, -NH2, stb) vannak kialakítva a más csoportba tartozó vegyületek: hidroxi, keto, aminosavak és mások.
Az általános képlet a határ egybázisú karbonsavak:
Az általános képletű telítetlen monokarbonsavak:
Az általános képlet a határ kétbázisú karbonsavak:
A nevek és néhány általános képletű karbonsavak
A három azonos csövek nélkül aláírások három savak: hangyasav, ecetsav és sósav. Mivel alapján különbségek a kémiai tulajdonságai határozzák meg, amely sav jelen van minden csőbe?
Hangyasav is mutat bizonyos tulajdonságait aldehidet (csökkenés). Ezért lehet meghatározni. például reagáltatva hidroxiddal réz (II), van kialakítva réz-oxid esetében a hangyasav (I) Piros:
Meg tudja különböztetni a maradék savat ezüst-nitráttal reagáltatjuk. Abban az esetben, sósav, fehér ezüst-klorid csapadékot:
Ezüst-acetát vízben oldható, így az in vitro ecetsavval változás fog bekövetkezni.
Így a maradék csövet - ecetsav.
Határozza képletű észtert. ha annak hidrolízis tömegű mintát 2,64 g osztják 1,38 g alkoholt és 1,8 g egybázisú karbonsav.
Az általános képlet szerinti észter álló alkohol és sav különböző szénatomokhoz:
Így egy általános képletű alkoholt:
sav és a képlet:
Az egyenlet hidrolízisének észter:
Összhangban a törvény tömeg megmaradási anyagok, súlya a reakciótermékek megegyezik a tömege a kiindulási anyagok. Kiszámítjuk a víz tömege:
m (sav) + m (alkohol) - m (észter) g
Kiszámítjuk a víz mennyisége anyag:
Szerint a reakció egyenlet
n (sav) = N (alkohol) mol
Találunk moltömegére az alkohol és a sav:
Azt találjuk, az együtthatók m és n a sav és egy általános képletű alkohol:
Formula sav CH3COOH - ecetsav
Formula-alkohol C2 H5 OH - etanol.
Így, a képlet az észter CH3 COOC 2H 5 - etil-acetát, etil-acetát.